Im regulierten Life Sciences-Umfeld kommt der Verwaltung kontrollierter Dokumente wie beispielsweise SOPs (Standard Operating Procedures), Verfahrensanweisungen oder Arbeitsweisungen eine große Bedeutung zu. Change Management-Prozesse sichern die ordnungsgemäße Überarbeitung, Genehmigung, Schulung, Verteilung und ggf. Außerkraftsetzung dieser Dokumente. Neben allseits bekannten Use Cases innerhalb des Change Managements existieren Sonderfälle, die von Unternehmen zu Unternehmen andersartig ausgestaltet werden.
Einer dieser Anwendungsfälle ist der Vorgang der Dokumentenfreigabe.
Fallbeispiel
Die Arbeitsanweisung für einen neuen Flüssigkeitschromatographen, mit dem Substanzen physikalisch voneinander getrennt werden können, durchläuft einen elektronischen Genehmigungsprozess mithilfe eines unternehmenseigenen Dokumentenmanagementsystems (DMS). Abhängig von den individuellen Unternehmensrichtlinien signieren Dokumentenkoordinatoren, Betriebsleiter oder Qualitätsbeauftragte die Arbeitsanweisung auf elektronischem Wege. Am 1. Oktober ist das Signieren erfolgreich abgeschlossen und das DMS stellt sicher, dass die Arbeitsanweisung im DMS den Status »Genehmigt« erhält. Gleichzeitig ändert das DMS die Zugriffsrechte auf das Dokument: Schreibzugriff wird entzogen und Lesezugriff ausschließlich den Dokumentenkoordinatoren und Qualitätsbeauftragten erteilt. – Das Dokument ist nun genehmigt.
Wie im Falle vieler anderer, kritischer Dokumentarten auch, muss das Personal, das die Arbeitsanweisung im späteren Arbeitsalltag benutzen wird, nun entsprechend geschult werden: Nicht nur der Inhalt der Arbeitsanweisung, sondern auch der Umgang mit dem zugrundeliegenden Flüssigkeitschromatographen muss umfangreich trainiert werden. Hierzu ist es notwendig, das Gerät nach seiner Beschaffung beispielsweise in einem Technikum aufzubauen und einen Versuchsstand herzurichten. Die Schulung muss organisiert und das Personal eingeladen werden. Am 1. November sind all diese Vorbereitungen erfolgt und ein Dokumentenkoordinator stellt im DMS den Status der Arbeitsanweisung von »Genehmigt« auf »Freigegeben« um. Das DMS ändert erneut die Zugriffsrechte: Zusätzlich zu Dokumentenkoordinatoren und Qualitätsbeauftragten erteilt das DMS nun auch allen Schulungsteilnehmern und späteren Nutzern Lesezugriff. Jeder Mitarbeiter, der die Schulung durchläuft und im späteren Arbeitsalltag mit der Arbeitsanweisung arbeiten wird, kann nun das Dokument im DMS einsehen oder einen Druckvorgang anstoßen, um sich in das Dokument einzuarbeiten.– Das Dokument ist nun freigegeben.
Nach mehreren Wochen hat das gesamte Personal die Schulung durchlaufen. Der Flüssigkeitschromatograph ist in dem jeweiligen Labor installiert und löst dort beispielsweise ein veraltetes Gerät ab. Der Laborleiter legt in Zusammenarbeit mit einem Qualitätsbeauftragten den 1. Dezember als Stichtag fest: Ab diesem Zeitpunkt darf das Laborpersonal nur noch das neue Gerät benutzen. Gleichzeitig legt ein Dokumentenkoordinator im DMS den 1. Dezember als Gültigkeitsdatum (oder Effektivdatum) für die zugehörige Arbeitsanweisung fest. Das DMS stellt an diesem Stichtag den Dokumentenstatus von »Freigegeben« auf »Gültig« (oder »Effektiv«) um.
Das DMS stellt durch entsprechende Zugriffsrechte weiterhin sicher, dass eventuelle Vorgängerversionen der Arbeitsanweisung für Endnutzer nicht mehr sichtbar sind. Ausschließlich die gültige (oder effektive) Version des Dokuments darf von diesem Stichtag an benutzt werden. Jeder Ausdruck, den ein Nutzer von nun an anstößt, wird vom DMS automatisch protokolliert (kontrolliertes Drucken). – Das Dokument ist nun gültig.
Die chronologische Abfolge der Dokumentenfreigabe findet in diesem Fallbeispiel also wie folgt statt:
1. Oktober: Dokument vollständig genehmigt (approved). Alle Verantwortlichen leisteten ihre Unterschrift.
1. November: Dokument freigegeben (released). Das Dokument kann von nun an von Endnutzern eingesehen werden.
1. Dezember: Dokument gültig (effective). Von nun an muss das Dokument genutzt werden.
Lösung aus Anwendersicht (Auszug)
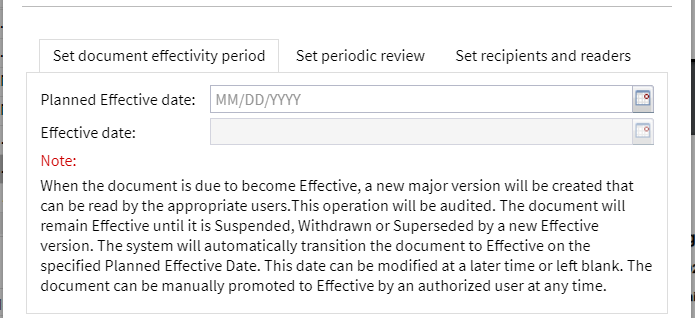
Alle Unterzeichner signieren das Dokument auf elektronischem Wege innerhalb des DMS mit Hilfe eines Approval Workflows. Am Ende des Genehmigungsprozesses legt ein Dokumentenkoordinator das geplante Gültigkeitsdatum fest. Falls dieses zum Zeitpunkt der Genehmigung noch nicht feststeht, kann es zu einem späteren Zeitpunkt festgelegt werden (s.u.).
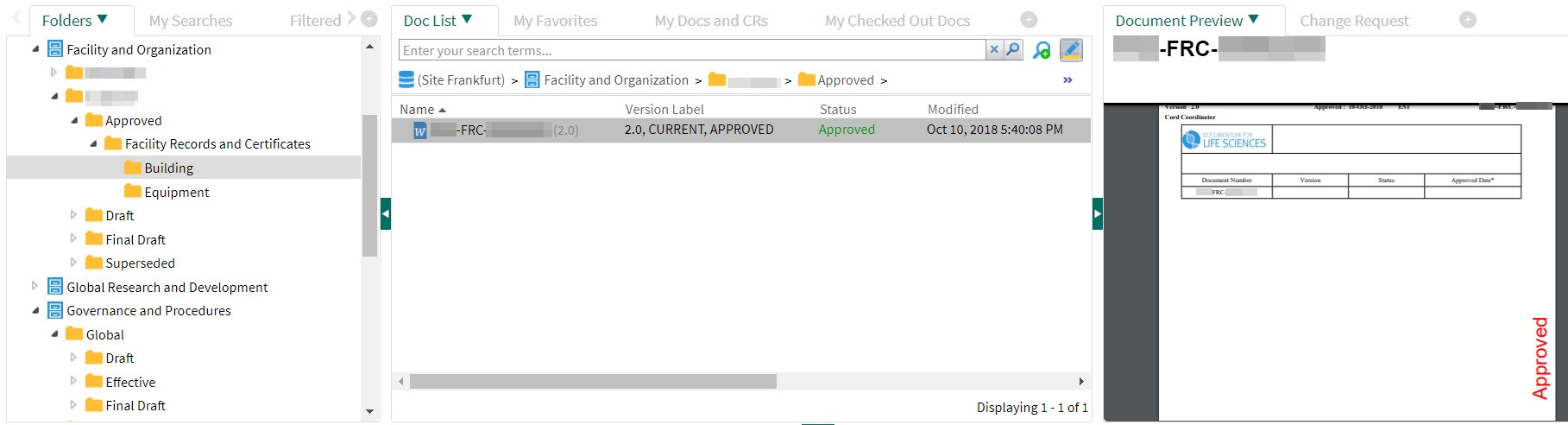
Das Dokument ist nun genehmigt und wird im DMS entsprechend dargestellt:
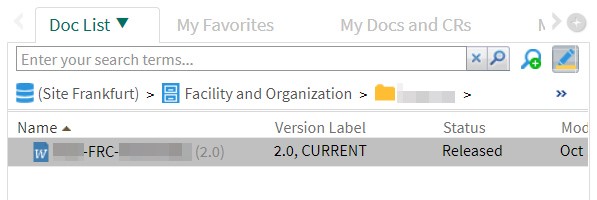
Sobald ein Dokumentenkoordinator das Dokument freigibt, ändert das DMS den Dokumentenstatus (»Released«) und passt die Zugriffsberechtigungen entsprechend an:
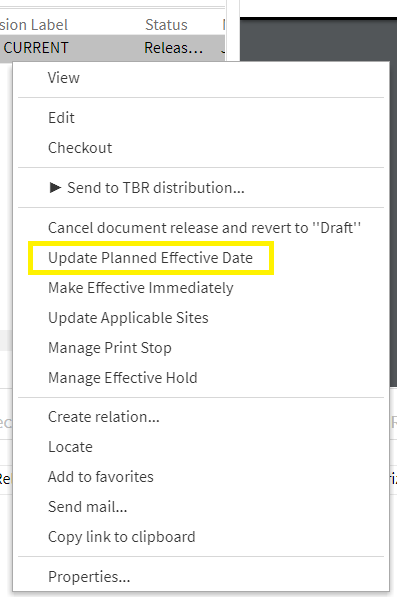
Nach erfolgreicher Schulung und Abschluss aller Vorbereitungen, legt der Dokumentenkoordinator das Gültigkeitsdatum fest. Wurde das Gültigkeitsdatum bereits festgelegt (s. o.), so kann es nachträglich geändert werden; alternativ kann dieser Schritt übersprungen werden:
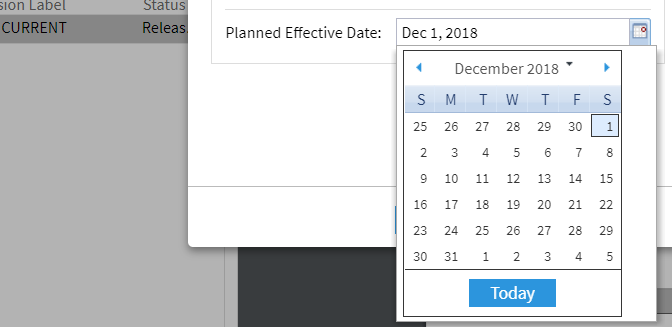
Das DMS stellt sicher, dass das Dokument am 1. Dezember in den Status »Gültig« (»Effective«) überführt wird inklusive geänderter Zugriffsberechtigungen.
Technische Implementierung (Auszug)
Der skizzierte Geschäftsprozess kann auf Basis von OpenText Documentum for Life Sciences implementiert werden. Die detaillierten Kundenanforderungen können in diesem Anwendungsfall sehr unterschiedlich ausfallen.
Die OpenText Life Sciences Lösung bietet standardmäßig für sogenannte Kategorie 1-Dokumente ein zweistufiges Freigabeverfahren: Ein Dokument wird nach seiner vollständigen Genehmigung in den Gültigkeitsstatus überführt. Ein separater »Freigegeben«-Status zwischen »Genehmigt« und »Gültig« existiert nicht (Zu beachten: Innerhalb der Life Sciences Lösung wird der Zustand »Genehmigt« als »Freigabe ausstehend” bezeichnet. Der Wortlaut mag etwas verwirrend sein, aber »Freigabe ausstehend« und »Freigegeben« dürfen nicht verwechselt werden!)
Kategorie 2- und Kategorie 3-Dokumente besitzen keinen »Gültig«, sondern lediglich einen »Genehmigt«-Status.
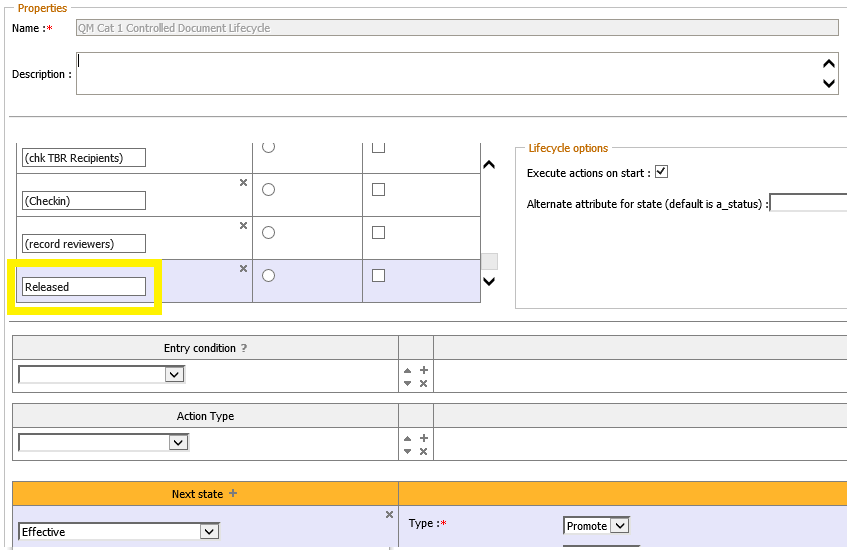
Abhängig von der Kundenanforderung muss zur technischen Realisierung der »QM Cat 1 Controlled Document Lifecycle« angepasst werden. Ein zusätzlicher Status »Released« kann vor den bestehenden »Effective«-Status eingefügt werden, jedoch erfordert diese Maßnahme sehr gute Kenntnisse in der Funktionsweise der Life Sciences Lösung.
Sie haben Fragen oder wünschen weitere Informationen?
Füllen Sie einfach unser Kontaktformular aus oder besuchen Sie unsere OpenText Documentum for Life Sciences Landingpage.
Hier finden Sie die Teile eins bis drei meiner Blogpost-Serie »Spezielle Anwendungsfälle auf Basis von OpenText Documentum for Life Sciences«:
The Extremely Efficient Effectivity Hold
The Mysterious Case of TDC
A Contribution to Controlled Printing






0 Kommentare